理学研究科_全体の傾向

まずは全体の傾向から知りたい!
続いて、大阪大学大学院理学研究科の過去問分析結果を説明します。
まずは全体の傾向をざっくり掴んでおきましょう。
下図に阪大大学院理学研究科の物理化学の各単元の出題割合をまとめました。
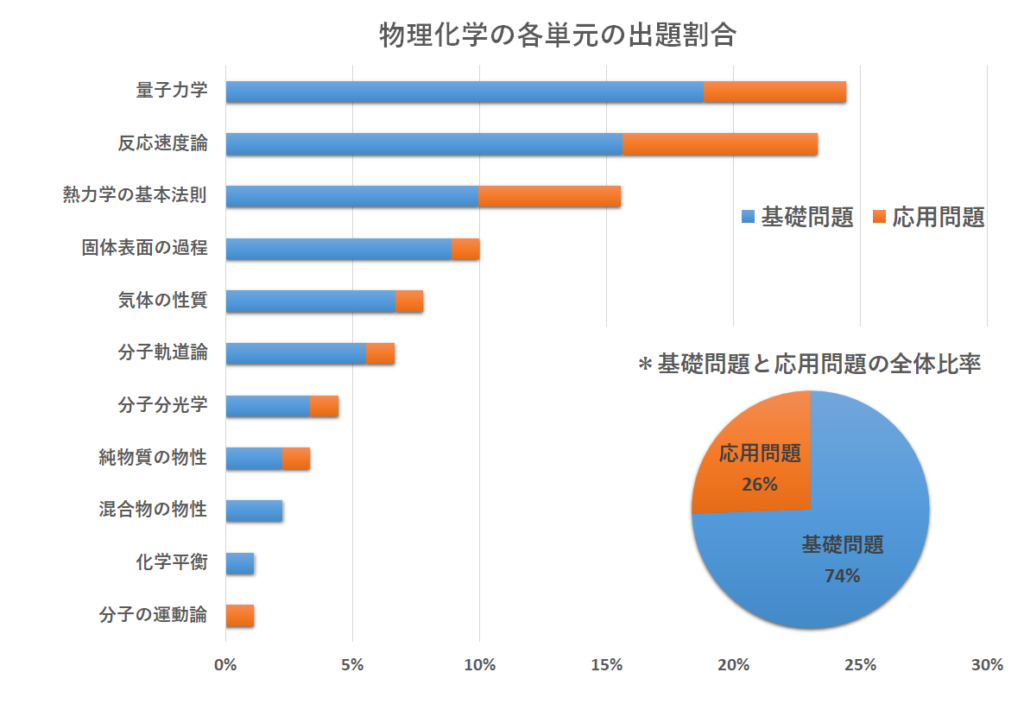
様々な単元から出題されていますが、量子力学・反応速度論・熱力学の基本法則に関する問題で約6割を占めています。
阪大大学院理学研究科の物理化学はこれらの単元を重要視しているようですね。
また、基礎問題と応用問題の比率を見てみると、全体としては74%が基礎問題で26%が応用問題です。
つまり、阪大大学院理学研究科の物理化学は工学研究科に比べるとやや難しいですが、基礎問題が中心であることは確かです。
教科書レベルの基礎事項をまずはしっかり理解するのが有効な対策ですね。
次節から具体的な対策方法を解説いたします。

【大学院入試の過去問分析】化学専攻必見!物理化学の頻出問題を解説で述べた全体の傾向と比較すると、頻出単元の傾向はよく一致しています。一方で、固体表面の過程が出題されるのは非常に珍しく、阪大大学院理学研究科の特徴ですね。
理学研究科_絶対に落とせない頻出問題


どんな問題が頻出なの?対策の仕方は?
各単元の頻出問題を下記にまとめました。
〇量子力学
・1次元箱型ポテンシャル中の粒子のエネルギー準位図作成と電子遷移に必要なE計算
・2次元箱型もしくは円環中の粒子のエネルギー準位図作成
・ある量子数の時の波動関数図示
〇反応速度論
・定常状態近似を用いた速度式立式(N2O5の分解反応、酵素反応など)
〇熱力学の基本法則
・理想気体の等温可逆変化および断熱可逆変化時の熱力学パラメータの変化計算
・化学反応に伴う熱力学パラメータの変化計算
〇固体表面の過程
・固体表面への理想気体の吸着過程
〇気体の性質
・ファンデルワールスの状態方程式
〇分子軌道論
・ヒュッケル近似を用いた共役ポリエンの分子軌道のエネルギー準位図作成
これらの頻出問題の対策は大部分が前記事【大学院入試の過去問分析】化学専攻必見!物理化学の頻出問題を解説で紹介済みですので、ぜひご覧ください。
一部未解説の問題について、下記に対策をまとめました。
・固体表面への気体吸着:吸着方法の種類と特徴、表面被覆率の変化を用いた吸着速度と脱着速度の表現、ラングミュア等温式の導出、吸着分子の体積を用いたラングミュア等温式の変形を押さえておく。
量子力学の未解説問題に関しては周りと差がつくポイントなので、次節で改めて解説します。
頻出問題は基礎問題が多いですので周りの受験生も当然対策済みです。
簡単な問題が答えられず差がつくことがないようにしっかり対策しておきましょう。

阪大大学院理学研究科の物理化学は問題数が他大学に比べて少ないです。1問1問丁寧に解答しましょう。最後に見直しをする時間を作り、ケアレスミスを防ぐのも合格する上で重要ですよ。
理学研究科_周りと差がつくポイントとは?


頻出問題は皆正解するからそれだけ押さえても合格することは難しいよね。他の受験者と差をつけるためにはどうしたらいいの?
他の受験者と差をつけるためには「応用問題を解けるようになる」「よく出題されるが周りがあまり対策していない単元を押さえておく」の2点が重要です。
この2点を踏まえて、さきほどの物理化学の各単元の出題割合の図をもう1度見てみましょう。
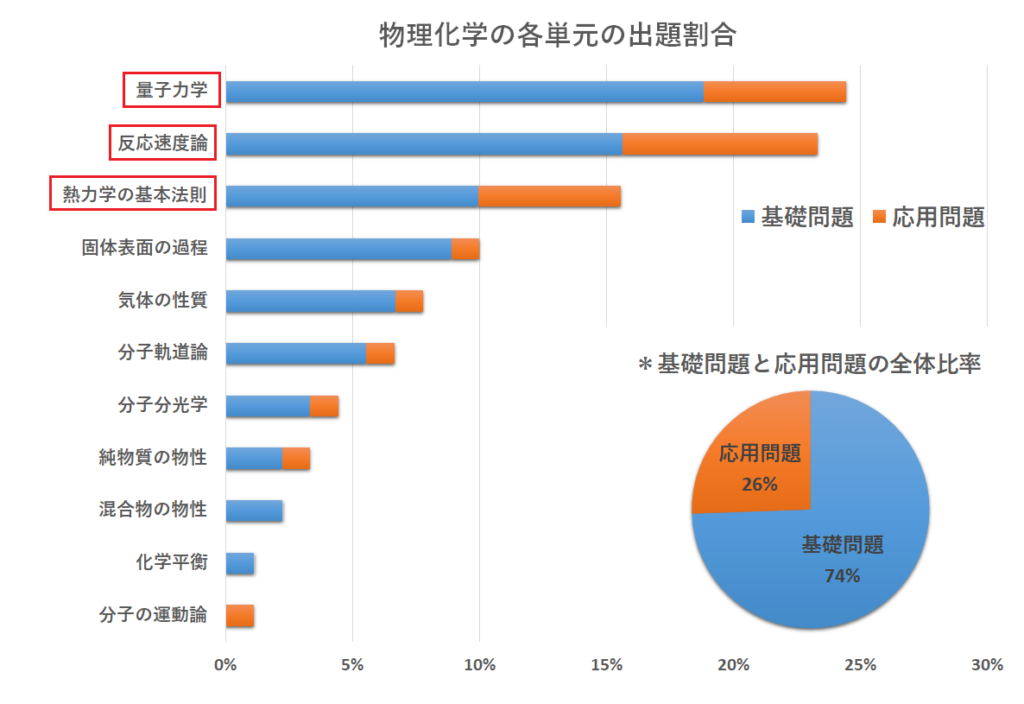
良く出題される上に応用問題の割合が高いのは「量子力学」「反応速度論」「熱力学の基本法則」ですね。
これらの単元に関しては幅広い知識と深い理解が必要であることが分かります。
また、阪大大学院理学研究科の物理化学は工学研究科と同様に複雑な関係式の導出を扱う応用問題が頻出です。
ただし、この手の応用問題は問題文の誘導に従えば見た目ほど難しくないことが多いですね。
すなわち、差がつくポイントは下記です。
①量子力学・反応速度論・熱力学の基本法則に関する幅広い知識と深い理解があるか?
②見た目のややこしさに惑わされずに基礎知識をもとに複雑な関係式を導けるか?
上記の問いに2つとも「Yes」と答えられる受験生が合格します。
どんな対策をすればいいのかを次節で見ていきましょう。

阪大大学院理学研究科の化学は前半が必須解答で後半が選択問題になっています。物理化学の選択問題は見た目は難しそうですが問題文に書かれた情報=ヒントを丁寧に処理すれば思ったより簡単です。物理化学が得意な方ならきっと完答できると思いますよ。
理学研究科_周りと差をつけるためにやるべきこと


差がつくポイントは分かったけど、具体的にどんな勉強をすればいいの?
周りの受験生と差をつけるためにどんな対策をすればいいのかを、実際の出題例を見ながら解説します。
①量子力学の対策
・基本的な1次元空間中の粒子のシュレーディンガー方程式を解き、エネルギー準位図を作成するまでの流れをマスターする
・エネルギー準位図から分かること(電子遷移に必要なエネルギーやゼロ点エネルギーなど)を把握しておく
・各量子数における波動関数の形状(どこに節があるか)を覚えておく
・2次元空間中の粒子のシュレーディンガー方程式の解法も調べておく
*具体的には下記のような出題例あり
例)1,3,5-ヘキサトリエンのHOMO-LUMO遷移に伴う光吸収の波長計算、基底状態から第1励起状態へ励起するのに必要なエネルギー計算、励起するのに必要なエネルギーを半分にする方法を考察、箱の長さが変化したときのエネルギー準位図の変化を考察、ベンゼンのHOMO-LUMOのエネルギー差計算、2次元円環内の電子と1次元箱内の電子のゼロ点エネルギーの比較、1次元箱型ポテンシャル中の粒子の波動関数図示、2次元箱型ポテンシャル中の粒子の波動関数図示、量子数と節の個数の関係を考察
②反応速度論の対策
・教科書に出てくる典型的な定常状態近似を用いた反応速度式導出は自分で1からできるようになっておく
・阻害過程が存在する場合の酵素反応の速度式導出方法を勉強しておく
・アレニウスの式の意味や利用法を勉強する
*具体的には下記のような出題例あり
例)N2O5の分解反応について定常状態近似を用いて速度式導出、ミカエリス・メンテン式導出、拮抗阻害がある場合の酵素反応の速度式導出、反拮抗阻害がある場合の酵素反応の速度式導出、拮抗阻害と反拮抗阻害が両方ある場合の酵素反応の速度式導出、オゾン層形成の純酸素化学平衡モデルにおけるオゾン濃度を定常状態近似で導出、アレニウスの式を使って重水素置換前後の反応速度定数の比を導出
③熱力学の基本法則の対策
・各パラメータ(T、P、V、q、w、U、Cv、Cp、H、S、A、G)の間に成り立つ関係式を体系的に理解する
・等温可逆変化および断熱可逆変化時にはどの熱力学パラメータが不変なのかに注意して、ΔU・ΔH・ΔS・ΔGの導出方法を理解しておく
・反応に伴う熱力学パラメータ変化は各反応物の生成エネルギーや反応に関与する結合エネルギーから計算できることを把握しておく
・カルノーサイクルやマクスウェルの関係式といった科学者の名前がついている理論は問題にされやすいので調べておく
*具体的には下記のような出題例あり
例)断熱容器にアルゴンを注入した際の系のU、理想気体を断熱可逆圧縮した際のΔU、理想気体を等温可逆膨張させた際のΔHとΔS計算、反応のΔGを各反応物の生成のΔGから計算、反応のΔHを反応に関与する結合エネルギーや反応物の生成のΔHから計算、Hに関するマクスウェルの関係式導出
④見た目のややこしさに惑わされず、問題文をよく読み、誘導に丁寧に従う
・基礎事項から問題が始まり、ヒントをもとに複雑な関係式を導く問題へ発展する流れが多い
・いきなり問題を解くより先に問題文全文を読んで問題の全体像を把握した方が解きやすい
・途中の問題が分からなくてもそれ以降で解答できる問題もあるのであきらめない
差がつくポイントまで押さえておけば合格は目の前ですよ!

物理化学の計算問題は最後まで式変形した後に数値を代入して計算するのをおススメします。式変形前に数値を代入して計算すると、余分な計算までしてしまう可能性があり、計算ミスする機会が増えますからね。
理学研究科_まとめ
いかがでしたでしょうか?最後におススメの勉強手順を示します。
Step 1:量子力学・反応速度論・熱力学の基本法則に該当する教科書の章および授業ノートを復習
Step 2:量子力学・反応速度論・熱力学の基本法則に関して本記事の頻出問題や差がつくポイントを勉強
Step 3:教科書の例題や授業中の演習問題を解けるようになる
Step 4:時間が許す限り他単元も出題割合の高い順に同様の流れで勉強
Step 5:過去問演習(直近5年分)&復習
上記のステップに沿って勉強すれば、阪大大学院理学研究科の物理化学対策は十分ですよ!
最後に
大学受験では大阪大学は難しいイメージがありますよね。
一方で、大阪大学大学院の入試は難しいわけではありません。
教科書レベルの知識をそのまま問う問題がほとんどです。
ただし、阪大大学院は受験者のレベルが高いので、本記事で述べた差がつくポイントまでしっかり押さえておくことが合格する上で重要です。
本記事と合わせて、阪大大学院の有機化学・無機化学の対策の記事も合わせて読んでくださいね。
以上、ご参考になれば幸いです。





























コメント